Contoh soal kesetimbangan kimia nomor 1
Suatu reaksi kesetimbangan:
2 CO (g) + O2 (g) ⇄ 2 CO2 (g) ΔH = -x kJ/mol
Agar kesetimbangan bergeser ke kanan, hal-hal di bawah ini perlu dilakukan, kecuali …
A. Pada suhu tetap, konsentrasi gas CO ditambah
B. Pada suhu tetap, tekanan sistem diturunkan
C. Pada suhu tetap, volume diturunkan
D. Pada suhu tetap, konsentrasi gas oksigen ditambah
E. suhu diturunkan
Pembahasan
Soal ini jawabannya B. Karena jika tekanan diperkecil maka kesetimbangan akan bergeser ke arah jumlah koefisien reaksi besar.
Koefisien reaksi di kiri = 2 + 1 = 3 (besar)
koefisien reaksi di kanan = 2 (kecil)
Jadi, jika tekanan sistem diturunkan (diperkecil) maka kesetimbangan bergeser ke kiri karena koefisien reaksinya besar.
Contoh soal kesetimbangan kimia nomor 2
Dalam ruang tertutup, terdapat reaksi kesetimbangan:
H2 (g) + Cl2 ⇄ 2 HCl (g) ΔH = -92 kJ/mol
Jika suhu dinaikkan, maka kesetimbangan akan bergeser ke arah …
A. kiri, harga K bertambah
B. kiri, harga K berkurang
C. kiri, harga K tetap
D. kanan, harga K bertambah
E. kanan, harga K tetap
Pembahasan
Jika suhu dinaikkan maka kesetimbangan akan bergeser ke arah endoterm (kiri) dengan harga K tetap. Soal ini jawabannya C.
Contoh soal kesetimbangan kimia nomor 3
Pada reaksi kesetimbangan:
CO (g) + 3 H2 (g) ⇄ CH4 (g) + H2O (g)
tetapan kesetimbangan untuk reaksi tersebut adalah ….
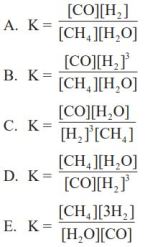
Pembahasan
Soal ini jawabannya D.
Contoh soal kesetimbangan kimia nomor 4
Dalam volume 5 liter terdapat 4,0 mol asam iodida, 0,5 mol yodium dan 0,5 mol hidrogen dalam suatu kesetimbangan. Maka tetapan kesetimbangan untuk reaksi pembentukan asam iodida dari iodium dan hidrogen adalah …
A. 50
B. 54
C. 56
D. 60
E. 64
Pembahasan
Reaksi: I2 (g) + H2 (g) ⇄ 2HI (l)
→ [I2] =→ [H2] =
→ [HI] =
→ K =
→ K =
Soal ini jawabannya E.
Contoh soal kesetimbangan kimia nomor 5
Dalam ruang 4 liter terdapat reaksi kesetimbangan:
NO2 (g) + CO (g) ⇄ NO (g) + CO2 (g)
Jika pada saat setimbang terdapat gas NO2 dan gas CO masing-masing 0,2 mol, dan gas NO serta CO2 masing-masing 0,4 mol, maka besarnya tetapan kesetimbangan pada suhu tersebut adalah …
A. 0,25
B. 0,5
C. 1
D. 2
E. 4
Pembahasan
→ [NO2] =→ [CO] =
→ [NO] =
→ [CO2] =
→ K =
→ K =
Soal ini jawabannya E.
Contoh soal kesetimbangan kimia nomor 6
Diketahui reaksi kesetimbangan:
2 CO (g) + O2 (g) ⇄ 2 CO2 (g)
Dalam ruang 2 liter direaksikan 5 mol CO dan 5 mol O2. Jika pada saat setimbang terdapat 4 mol gas CO2, maka besar Kc adalah …
A. 0,09
B. 1,067
C. 9
D. 10,67
E. 90
Pembahasan
→ [CO] =→ [O2] =
→ [CO2] =
→ Kc =
→ Kc =
Soal ini jawabannya D.
Contoh soal kesetimbangan kimia nomor 7
Dalam ruang 2 liter dicampurkan 1,4 mol gas CO dan 1,4 mol gas hidrogen menurut reaksi:
CO (g) + 3 H2 (g) ⇄ CH4 (g) + H2O (g)
Jika pada saat setimbang terdapat 0,4 mol gas CH4, maka harga Kc adalah …
A. 0,2
B. 0,8
C. 1,25
D. 8
E. 80
Pembahasan
→ [CO] =→ [H2] =
→ [CH4] =
→ [H2O] =
→ Kc =
→ Kc =
Soal ini jawabannya E.
Contoh soal kesetimbangan kimia nomor 8
Harga Kc untuk reaksi:
2 A2B (g) ⇄ 2 A2 (g) + B2 (g)
adalah 16. Pada suhu 27 oC, besarnya Kp untuk reaksi tersebut adalah…
A. 35,4
B. 246
C. 300,3
D. 393,6
E. 412
Pembahasan
T = (27 + 273) K = 300 K
Koefisien kanan = 2 + 1 = 3
koefisien kiri = 2
Δn = 3 – 2 = 1
Kp = Kc = (RT)Δn
Kp = 16 (0,082 x 300)1 = 393,6
Soal ini jawabannya D.
Contoh soal kesetimbangan kimia nomor 9
Pada saat suhu t oC gas NO dan gas O2 masing-masing sebanyak 3 mol dicampurkan dan bereaksi membentuk 2 mol gas NO2 menurut reaksi:
2 NO (g) + O2 (g) ⇄ 2NO2 (g)
Jika tekanan total = 2 atm, maka harga Kp adalah …
A. 1/4
B. 1
C. 2
D. 5
E. 8
Pembahasan
Jumlah mol setimbang = 1 + 2 + 2 = 5
→ PNO =→ PO2 =
→ PNO2 =
→ Kp =
→ Kp =
Soal ini jawabannya D.
Contoh soal kesetimbangan kimia nomor 10
Dalam ruang 1 liter terdapat reaksi kesetimbangan:
2 HI (g) ⇄ H2 (g) + I2 (g)
Bila mula-mula terdapat 0,4 mol HI, dan diperoleh 0,1 mol gas hidrogen pada saat setimbang, maka besarnya derajat disosiasi HI adalah …
A. 0,25
B. 0.50
C. 0,60
D. 0,75
E. 0,80
Pembahasan
→ α =→ α =
Soal ini jawabannya B.